
Con un Valor Predictivo Negativo (VPN), sensibilidad y especificidad del 100%, 100% y 55.2% respectivamente para la exclusión de la TVP y del 99.7%, 97.0% y 75.5% respectivamente para la exclusión del EP, el STA®-Liatest® D-Di demuestra las mejores características (best-in-class) clínicas de los D-dimeros automatizados para la exclusión de la TVP y del EP con los más rigurosos requerimientos para un estudio exhaustivo y prospectivo cumpliendo las guidelines CLSI H59-A, Quantitative D-Dimer for the exclusion of venous thromboembolic disease, aprobadas en 2011.
Durante más de 15 años el STA®-Liatest® D-Di ha sido el standard de la clínica para cuantificar y automatizar los análisis de D-dimero en miles de hospitales, centros médicos y laboratorios privados con más de 2 millones de resultados de pacientes reportados a nivel mundial. Los resultados del D-dimero son fundamentales en el algoritmo diagnóstico para la exclusión del TromboEmbolismo Venoso (TEV) en pacientes con probabilidad pre-test baja o moderada. El uso de los resultados de D-dimero está indicado por el documento CLSI H59-A, Quantitative D-Dimer for the exclusion of venous thromboembolic disease, guideline aprobado y publicado in 2011.
Para demostrar la fiabilidad del rendimiento clínico y el cumplimiento de los rigurosos requerimientos de las guías CLSI, Stago realizó un estudio prospectivo de 5 años, multinacional, incluyendo la evaluación de probabilidad pre-test, resultados de diagnóstico por imagen y tres meses de seguimiento de los pacientes: el estudio DIET, registrado en el US National Institutes of Health (NCT01221805).
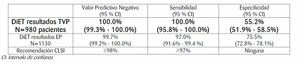
Más de 2000 pacientes ambulatorios con sospecha de TVP o EP se enrolaron en el estudio DiET en 16 centros a nivel mundial: Estados Unidos (9), Canadá (1), Francia (2), Italia (2) y España (2). Los resultados excedieron los objetivos de evaluación requeridos por la FDA y la CLSI para la Sensibilidad y Valor Predictivo Negativo (VPN), los dos criterios más relevantes para la exclusión de la TVP y del EP en pacientes con baja o moderada probabilidad pre-test como se indicaba en la CLSI H59-A.
STA®-Liatest® D-Di también ha demostrado la mejor (best-in-class) especificidad clínica en el estudio DiET. Una alta especificidad indica menos resultados falsos positivos de D-dimero y por tanto menos estudios innecesarios de diagnóstico por la imagen que incrementan el coste del tratamiento del paciente, el tiempo de hospitalización y la exposición del paciente a radiación y complicaciones asociadas a los estudios de imagen.
El STA®-Liatest® D-Di y STA®-Liatest® D-Di Plus ofrecen resultados fiables, totalmente automatizados y reactivos listos para su uso, con la mejor eficiencia gracias a los 15 dias de estabilidad en equipo, nuevos controles líquidos con 72 horas de estabilidad en equipo y resultados en 8 minutos.

